Información para l@s alumn@s y familias:
- Criterios de evaluación y contenidos 4º Física y Química
- Contenidos oficiales Comunidad de Madrid 4ºESO Física y Química
- Indicadores observables y evaluables
- Rúbrica de valoración del cuaderno de clase
- Informe prácticas de laboratorio
- Compromiso del alumno en el laboratorio
- Reflexiona sobre lo aprendido con los estándares evaluables de aprendizaje
- Comentarios y evaluación docente
- Currículo oficial de Secundaria de la Comunidad de Madrid
Apuntes 4º ESO en pdf:
- Actividad Científica
- Magnitudes
- El átomo
- Teorías atómicas
- Sistema periódico
- Enlace Químico
- Sistema periódico y enlace, Sistema periódico y enlace (II)
- Nomenclatura inorgánica
- Nomenclatura orgánica
- Reacciones químicas
- Concepto de mol
- Cálculos estequiométricos
- Cálculos químicos
- Cinemática
- Movimiento rectilíneo uniforme
- Movimiento rectilíneo uniformemente acelerado
- Movimiento circular uniforme, Movimiento circular uniforme (II)
- Dinámica, Dinámica (II)
- Gravitación Universal
- Modelos cosmológicos
- Posición de la Tierra en el Universo
- Gravitación
- Teoría de fluidos
- Flotación de cuerpos
- Presión y fluidos
- Trabajo y energía, Trabajo y energía (II)
- Calor y energía, Calor y energía (II), Calor y energía (III)
- General Física y Química
Presentaciones 4º ESO en pdf:
Libro de consulta donado de la editorial ELZEVIR (Refuerzo y Ampliación)
Hojas de ejercicios
- La investigación científica
- Cambio de unidades. Magnitudes. Cifras significativas
- Magnitudes, errores y método científico
- Estudio del movimiento
- Cinemática: MRU, MRUA
- Movimiento circular uniforme: MCU
- Composición de fuerzas
- Dinámica
- Fuerzas y dinámica
- Gravitación,
- Movimiento circular y gravitación
- Fuerzas y presión en los fluidos
- Energía y trabajo
- El átomo
- Tabla periódica y propiedades periódicas,
- Tabla periódica I
- Tabla periódica II
- Enlace químico I
- Enlace químico II
- Nomenclatura inorgánica, Binarios S, Ternarios S,
- Formulación y nomenclatura inorgánica, Binarios, Ternarios.
- Ajuste de reacciones I
- Ajuste de reacciones II
- Estequiometría I
- Estequiometría II
- Reacciones químicas
- Formulación y nomenclatura orgánica I
- Formulación y nomenclatura orgánica II
Hojas de ejercicios (Refuerzo y Ampliación)
- Teorías atómicas
- Átomos, sistema periódico y enlace
- Enlace químico
- Moles, moléculas y átomos
- Cálculos químicos
- Estequiometria
- Cinemática
- Tiro vertical y caída libre
- Cinemática y dinámica
- Dinámica I, Dinámica II, Dinámica III
- Gravitación I, Gravitación II
- Estática de fluidos
- Trabajo, potencia y energía
- Energía y trabajo
- Calor y energía
INVESTIGACIÓN CIENTÍFICA
La investigación científica, nos ayuda a mejorar el estudio porque nos permite establecer contacto con la realidad a fin de que la conozcamos mejor. Constituye un estímulo para la actividad intelectual creadora. La Investigación es un proceso que, mediante la aplicación del método científico, procura obtener información relevante, para entender, verificar, corregir o aplicar el conocimiento.
El método científico consta de las siguientes fases: identificación del problema, formulación de hipótesis, comprobación de hipótesis, extracción de conclusiones y comunicación de resultado.
ACTIVIDAD: Método Científico
ACTIVIDAD: Fases del Método Científico
EJERCICIOS DE INVESTIGACIÓN CIENTÍFICA
ACTIVIDAD: Fases del Método Científico
EJERCICIOS DE INVESTIGACIÓN CIENTÍFICA
En este vídeo se explica el método científico y sus etapas:
Una magnitud física es toda propiedad de los cuerpos que puede ser medida.
ACTIVIDAD: Magnitudes y unidades
Un factor de conversión es una fracción igual a la unidad que expresa la equivalencia entre dos unidades.
Un número expresado en notación científica estará formado por un número decimal con una parte entera de una sola cifra distinta de 0, multiplicado por una potencia de 10 de exponente entero.
ACTIVIDAD: Notación científica y potencias de 10
El error absoluto de una medida es la diferencia, en valor absoluto, entre el valor aproximado obtenido en la medición y el valor verdadero o exacto de la medida. Se expresa en las mismas unidades que la magnitud medida.
El error relativo de una medida es el cociente entre el error absoluto y el valor verdadero o exacto de la medida. No tiene dimensiones y determina el error que se comete por cada unidad de la magnitud medida.
El error relativo de una medida es el cociente entre el error absoluto y el valor verdadero o exacto de la medida. No tiene dimensiones y determina el error que se comete por cada unidad de la magnitud medida.
Las cifras significativas de una medida son todas las que se conocen con certeza, más una dudosa, es decir, que tiene un margen de error.
Una medida experimental se expresa mediante un intervalo determinado por el valor numérico obtenido, con todas sus cifras significativas, y el error absoluto correspondiente, que supondremos igual a la resolución del instrumento de medidad.
Una medida experimental se expresa mediante un intervalo determinado por el valor numérico obtenido, con todas sus cifras significativas, y el error absoluto correspondiente, que supondremos igual a la resolución del instrumento de medidad.
Algunos de los instrumentos y productos que se utilizan en el laboratorio pueden resultar peligrosos si no se manipulan correctamente. Para evitar riesgos, deberemos respetar siempre las normas de seguridad y observar los símbolos que aparecen en la etiqueta de los envases.
ACTIVIDAD: "Material de Laboratorio"
ACTIVIDAD: El Laboratorio y el Informe
CINEMÁTICA: EL MOVIMIENTO
Las magnitudes fundamentales para estudiar el movimiento de un cuerpo son el tiempo, la posición, la velocidad y la aceleración.
Cuando un objeto se mueve en línea recta decimos que su movimiento es rectilíneo. Si este movimiento es siempre a la misma velocidad, se llama movimiento rectilíneo uniforme (MRU).
ACTIVIDAD I: Introducción a la Cinemática
Cuando un objeto se mueve en línea recta decimos que su movimiento es rectilíneo. Si este movimiento es siempre a la misma velocidad, se llama movimiento rectilíneo uniforme (MRU).
Si, por el contrario, el movimiento está acelerado y está aceleración es siempre la misma, se denomina movimiento rectilíneo uniformemente acelerado (MRUA).
ACTIVIDAD III: Ejemplos de MRU y MRUA
ACTIVIDAD IV: Cinemática y Movimiento MRU
Decimos que un cuerpo realiza un movimiento circular uniforme (MCU) cuando su trayectoria es una circunferencia y su velocidad angular es constante, parámetros característicos de este movimiento es el período y la frecuencia.Recuerda las magnitudes fundamentales para estudiar el movimiento de un cuerpo son el tiempo, la posición, la velocidad y la aceleración.
Cuando un objeto se mueve en línea recta decimos que su movimiento es rectilíneo. Si este movimiento es siempre a la misma velocidad, se llama movimiento rectilíneo uniforme (MRU).
ACTIVIDAD I: MRU: Movimiento Rectilíneo Uniforme
ACTIVIDAD II: MRUA: Movimiento Rectilíneo Uniformemente Acelerado
Cuando un objeto se mueve en línea recta decimos que su movimiento es rectilíneo. Si este movimiento es siempre a la misma velocidad, se llama movimiento rectilíneo uniforme (MRU).
Si, por el contrario, el movimiento está acelerado y está aceleración es siempre la misma, se denomina movimiento rectilíneo uniformemente acelerado (MRUA).
ACTIVIDAD III: Ejemplos de MRU y MRUA
ACTIVIDAD IV: Cinemática y Movimiento MRU
ACTIVIDAD V: Cinemática y Movimiento MRUA
Repasa las siguientes actividades y simulaciones, relacionadas con los movimientos rectilíneo uniforme y movimiento rectilíneo uniformemente acelerado
Decimos que un cuerpo realiza un movimiento circular uniforme (MCU) cuando su trayectoria es una circunferencia y su velocidad angular es constante, parámetros característicos de este movimiento es el período y la frecuencia.
La composición de movimientos se basan en dos principios:
- Principio de Independencia: Cuando un móvil está sometido por causas diferentes a dos movimientos simultáneamente, su cambio de posición es independiente de considerarlos simultáneos o sucesivos
- Principio de superposición: La posición, velocidad y aceleración vienen dados por la suma vectorial de los movimientos parciales.
MOVIMIENTO CIRCULAR UNIFORME
Imagen de HereToHelp
El movimiento circular uniforme (M.C.U.) es el que describe un cuerpo que se mueve alrededor de un eje de giro con un radio y una velocidad angular (ω) constantes, trazando una circunferencia y con una aceleración centrípeta. En este movimiento, la dirección varia en cada instante. Un ejemplo de este movimiento es una rueda de automóvil que gira a una ω constante.
LAS FUERZAS: LEYES DE LA DINÁMICA
Una fuerza es toda acción capaz de producir alguna deformación en los cuerpos sobre los que actúa o alterar su estado de reposo o de movimiento. La dinámica es la rama de la física que describe la evolución en el tiempo de un sistema físico en relación con los motivos o causas que provocan los cambios de estado físico y/o estado de movimiento. El objetivo de la dinámica es describir los factores capaces de producir alteraciones de un sistema físico, cuantificarlos y plantear ecuaciones de movimiento o ecuaciones de evolución para dicho sistema de operación.
Las tres leyes de Newton son:
- Primera ley: Todo cuerpo mantiene su estado de movimiento hasta que actúa una fuerza sobre él
- Segunda ley: La aceleración que sufre un cuerpo es proporcional a la fuerza que actúa sobre él.
- Tercera ley: Cuando un cuerpo ejerce una fuerza sobre otro, recibe esa misma fuerza en sentido contrario.
La ley de la gravitación universal establece que entre dos cuerpos siempre existe una fuerza proporcional al producto de sus masas e inversamente proporcional al cuadrado de la distancia que los separa. Esta fuerza explica por qué los objetos pesan y por qué unos astros están orbitando en torno a otros. Para poder percibir está fuerza necesitamos que al menos uno de los objetos tenga una masa enorme (como la Tierra, la Luna o el Sol).
ACTIVIDAD IV: Astronomía y Gravitación
ACTIVIDAD V: Cálculo de la fuerza resultante
ACTIVIDAD VI: Construye una brújula
ACTIVIDAD VII: La vida de Newton
ACTIVIDAD VIII: Calcula tu peso en otros planetas
ACTIVIDAD VI: Construye una brújula
ACTIVIDAD VII: La vida de Newton
ACTIVIDAD VIII: Calcula tu peso en otros planetas
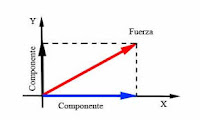
DESCOMPOSICIÓN DE FUERZAS
La descomposición de fuerzas es el proceso de representar una fuerza inclinada como la suma de dos fuerzas perpendiculares (componentes) que actúan en los ejes X e Y.
Se utiliza para simplificar los problemas al analizar el efecto de la fuerza en cada dirección por separado, empleando las razones trigonométricas (seno y coseno).
Método de descomposición
- Identifica los ejes: Se eligen dos ejes perpendiculares, usualmente el eje X (horizontal) y el eje Y (vertical), que se alinean con las direcciones de interés del problema.
- Proyecta la fuerza: Se "proyecta" la fuerza original sobre cada uno de los ejes para obtener las componentes X e Y. Esto se hace dibujando líneas perpendiculares desde el extremo de la fuerza hasta los ejes.
- Aplica la trigonometría: Para calcular el módulo de las componentes, se usan las razones trigonométricas:
- Componente en X (𝐹𝑥): 𝐹𝑥=𝐹⋅cos(𝜃)
- Componente en Y (𝐹𝑦): 𝐹𝑦=𝐹⋅sen(𝜃)
Donde: 𝐹 es el módulo de la fuerza original y 𝜃 es el ángulo que forma con uno de los ejes.
En este vídeo puedes ver un ejemplo en el que se suman fuerzas concurrentes:
LABORATORIO VIRTUAL DE DINÁMICA
La dinámica es una de las partes fundamentales de la Física, ya que nos permite entender por qué se mueven los cuerpos, cómo actúan las fuerzas y de qué manera influyen la masa, el rozamiento y la aceleración en el movimiento.
En los siguientes enlaces puedes ver simulaciones/ejercicios de dinámica explicados de forma clara y progresiva, pensados para estudiantes de ESO y Bachillerato. Los problemas están inspirados en los contenidos habituales de aula y en recursos educativos como Educaplus, e incluyen situaciones reales para facilitar la comprensión y el estudio
Actividad 1: Leyes de la dinámica
Actividad 2: Dinámica de la polea
Actividad 3: Dinámica de un bloque en un plano inclinado
Actividad 4: Ejercicio de dinámica 1
Actividad 5: Ejercicio de dinámica 2
Actividad 6: Ejercicio de dinámica 3
Actividad 7: Ejercicio de dinámica 4
Actividad 8: Ejercicio de dinámica 5
Actividad 9: Ejercicio de dinámica 6
LEY DE GRAVITACIÓN UNIVERSAL
Imagen propiedad de Wiki LIC
La ley de gravitación universal, formulada por Isaac Newton, establece que dos cuerpos con masa se atraen mutuamente con una fuerza directamente proporcional al producto de sus masas e inversamente proporcional al cuadrado de la distancia que los separa.
La fórmula matemática es:
F es la fuerza de atracción gravitatoria, G es la constante de gravitación universal, m1 y m2 son las masas de los dos objetos y r es la distancia entre los centros de los dos objetos.
Del enunciado podemos extraer estas particularidades:
- La fuerza gravitatoria es una fuerza de atracción: Todos los objetos con masa en el universo se atraen entre sí con una fuerza.
- Proporcionalidad directa con la masa: La magnitud de esta fuerza gravitatoria es mayor si las masas de los objetos son más grandes.
- Proporcionalidad inversa al cuadrado de la distancia: La fuerza disminuye al aumentar la distancia entre los cuerpos, siguiendo una relación de inverso del cuadrado.
- La fuerza gravitatoria actúa en la línea que une los centros de las masas: La fuerza actúa en la dirección del segmento de línea que une los centros de los dos cuerpos.
LAS LEYES DE KEPLER
Las Leyes de Kepler, que describen el movimiento de los planetas alrededor del Sol. Fueron formuladas por el astrónomo Johannes Kepler a principios del siglo XVII, y fueron importantes por los siguientes motivos:
- Confirmaron el modelo heliocéntrico de Copérnico.
- Sirvieron como base para que Newton formulara su Ley de Gravitación Universal
- Se aplican no solo a planetas alrededor del Sol, sino a cualquier cuerpo que orbite alrededor de otro bajo la influencia de la gravedad (por ejemplo, lunas alrededor de planetas).
Primera Ley de Kepler: Ley de las Órbitas
"Los planetas se mueven alrededor del Sol describiendo órbitas elípticas, donde el Sol ocupa uno de los focos de la elipse."
Explicación:
- Las órbitas no son circulares, sino elípticas (aunque en muchos casos son casi circulares).
- El Sol no está en el centro de la elipse, sino en uno de sus dos focos.
- Esto implica que la distancia entre el planeta y el Sol varía a lo largo de su órbita.
Segunda Ley de Kepler: Ley de las Áreas
"El radio vector que une un planeta con el Sol barre áreas iguales en tiempos iguales."
Explicación:
- El radio vector es la línea imaginaria que conecta el centro del planeta con el centro del Sol.
- Esta ley indica que el planeta se mueve más rápido cuando está más cerca del Sol (en el perihelio) y más lento cuando está más lejos (en el afelio).
- Es una consecuencia de la conservación del momento angular.
Tercera Ley de Kepler: Ley de los Períodos
"El cuadrado del período orbital de un planeta es directamente proporcional al cubo del semieje mayor de su órbita."
Explicación:
- Esta ley permite relacionar el tiempo que tarda un planeta en orbitar alrededor del Sol con su distancia media al mismo.
- Cuanto más lejos está un planeta del Sol, más tiempo tarda en completar su órbita.
FUERZA EN FLUIDOS
- La densidad del líquido.
- El valor de la gravedad.
- La profundidad o altura de la capa de líquido que hay por encima del punto considerado.
Actividad IV: Concepto de presión hidrostática
Actividad V: Calculo de la presión hidrostática
El Principio de Pascal nos indica que la presión ejercida sobre un líquido se transmite a todos sus puntos, en todas direcciones y sin perder intensidad.
Actividad VI: Principio de Pascal
La presión atmosférica es la fuerza que ejerce la atmósfera sobre cada metro cuadrado de superficie de la Tierra. Esta fuerza es el peso de la columna de aire que dicha superficie tiene encima, el primero que la midió fue Torricelli
Actividad VII: Experimento de Torricelli
El Principio de Arquímedes indica que todo cuerpo sumergido total o parcialmente en un fluido experimenta un empuje hacia arriba igual al peso del volumen del fluido desalojado.
Actividad VIII: Principio de Arquímedes
Actividad IX: Flotabilidad
Actividad X: Principio de Arquímedes
LA PRESIÓN HIDROSTÁTICA
La presión hidrostática es la presión que ejerce un fluido en reposo (líquido o gas) sobre un cuerpo sumergido o sobre las paredes del recipiente que lo contiene. Esta presión es el resultado del peso de la columna de fluido que se encuentra por encima del punto de medición.
La presión hidrostática (𝑃) se calcula mediante la expresión:
𝑃 = 𝜌⋅𝑔⋅ℎ
donde:
𝑃 = Presión hidrostática (en Pascales, Pa, en el Sistema Internacional)
𝜌 = Densidad del fluido (en 𝑘𝑔/𝑚3)
𝑔 = Aceleración debida a la gravedad (en 𝑚/𝑠2)
ℎ = Profundidad (o altura de la columna de fluido por encima del punto, en metros, m)
Conceptos clave
- Origen: Surge de la fuerza de la gravedad actuando sobre la masa del fluido. El peso del fluido es soportado por las capas inferiores, generando presión que aumenta con la profundidad.
- Dirección: En un fluido en reposo, la presión hidrostática actúa de manera perpendicular a todas las superficies de contacto (incluyendo las paredes del recipiente y cualquier objeto sumergido) y en todas direcciones.
- Dependencia: La presión hidrostática en un punto específico depende principalmente de tres factores, como se describe en el principio fundamental de la hidrostática:
- La densidad (𝜌) del fluido: A mayor densidad, mayor presión.
- La aceleración de la gravedad (g): En la Tierra se considera constante (9,8 N/kg).
- La profundidad (ℎ): A mayor profundidad, mayor es el volumen y peso del fluido por encima, por lo que la presión aumenta linealmente.
La presión hidrostática en un punto dentro de un fluido en reposo depende únicamente de la densidad del fluido (𝜌), la aceleración de la gravedad (𝑔) y la profundidad (ℎ) desde la superficie libre del fluido. No depende de la forma o el área del recipiente, un concepto clave en la hidrostática.
Vídeo demostración de la expresión de la presión hidrostática:
EL PRINCIPIO DE PASCAL
El principio de Pascal es una ley enunciada por el físico-matemático francés Blaise Pascal, que se resume en la frase:
"La presión ejercida sobre un fluido incompresible y en equilibrio dentro de un recipiente de paredes indeformables se transmite con igual intensidad en todas las direcciones y en todos los puntos del fluido."
Imagen propiedad de Darbyshmr
La prensa hidráulica es una máquina compleja que permite amplificar las fuerzas y constituye el fundamento de elevadores, prensas hidráulicas, frenos y muchos otros dispositivos hidráulicos.
La prensa hidráulica constituye la aplicación fundamental del principio de Pascal y también un dispositivo que permite entender mejor su significado. Consiste, en esencia, en dos cilindros de diferente sección comunicados entre sí, y cuyo interior está completamente lleno de un líquido que puede ser agua o aceite. Dos émbolos de secciones diferentes se ajustan, respectivamente, en cada uno de los dos cilindros, de modo que estén en contacto con el líquido. Cuando sobre el émbolo de menor sección A1 se ejerce una fuerza F1 la presión p1 que se origina en el líquido en contacto con él se transmite íntegramente y de forma casi instantánea a todo el resto del líquido. Por el principio de Pascal esta presión será exactamente igual a la presión p2 que ejerce el fluido en la sección A2.
EL PRINCIPIO DE ARQUÍMEDES
Propiedad de Imagen Principio Arquímedes
El principio de Arquímedes es el principio físico que afirma: "Un cuerpo total o parcialmente sumergido en un fluido en reposo experimenta un empuje vertical hacia arriba igual al peso del fluido desalojado". Esta fuerza recibe el nombre de empuje hidrostático o de Arquímedes, y se mide en newtons (en unidad fundamental el SI). El principio de Arquímedes se expresa mediante la siguiente fórmula:
E = Pe ·V=ρf · g ·V
o bien cuando se desea determinar para compararlo contra el peso del objeto:
E= −Pe ·V= −ρf · g ·V
donde E es el empuje, Pe es el peso específico del fluido, ρf es la densidad del fluido, V el volumen de fluido desplazado, por algún cuerpo sumergido parcial o totalmente en el mismo y g la aceleración de la gravedad. De este modo, el empuje depende de la densidad del fluido, del volumen del cuerpo y de la gravedad existente en ese lugar. El empuje (en condiciones normales y descrito de modo simplificado actúa verticalmente hacia arriba y está aplicado en el centro de gravedad del cuerpo; este punto recibe el nombre de centro de carena.
Ejemplo del principio de Arquímedes: "Ejercicio del iceberg"
TRABAJO Y ENERGÍA
El Principio de conservación de la energía indica que la energía no se crea ni se destruye; sólo se transforma de unas formas en otras. En estas transformaciones, la energía total permanece constante; es decir, la energía total es la misma antes y después de cada transformación.
En el caso de la energía mecánica se puede concluir que, en ausencia de rozamientos y sin intervención de ningún trabajo externo, la suma de las energías cinética y potencial permanece constante. Este fenómeno se conoce con el nombre de Principio de conservación de la energía mecánica.
Como la energía mecánica es igual a la suma de la energía cinética y la energía potencial gravitatoria que posee un cuerpo, la única forma de mantenerse constante es que:
- Cuando la energía cinética aumenta la energía potencial gravitatoria disminuye,
- Cuando la energía potencial gravitatoria aumenta la energía cinética disminuye.
ACTIVIDAD III: Trabajo y Energía Mecánica
PRINCIPIO DE CONSERVACIÓN
DE LA ENERGÍA MECÁNICA
Imagen propiedad de Por DemonDeLuxe
El principio de conservación de la energía mecánica establece que la energía mecánica total (suma de energía cinética y potencial) de un sistema se mantiene constante si solo actúan fuerzas conservativas (como la gravedad) y no hay fricción ni resistencia del aire, implicando que la energía se transforma entre cinética y potencial, pero su total no cambia. Si actúan fuerzas no conservativas (rozamiento), la energía mecánica disminuye, convirtiéndose en calor, aunque la energía total del universo se conserva.
Principio de conservación de la energía en un péndulo
En este vídeo se comenta el principio de conservación de la energía mecánica:
EL ÁTOMO Y LOS MODELOS ATÓMICOS

RESUMEN DEL TEMA: Átomos y Modelos Atómicos
RESUMEN DEL TEMA: Construyendo átomos
Este vídeo también te ayudará:
ACTIVIDAD I : El Átomo
Modelo de Dalton: Propone que los átomos están formados por esferas compactas e indivisibles. Explica adecuadamente los aspectos ponderales de las reacciones químicas, pero es insuficiente para explicar la naturaleza eléctrica de la materia.
ACTIVIDAD II : Modelo de Dalton
Modelo de Thomson: El átomo está formado por unas partículas con carga eléctrica negativa (electrones), inmersas en un fluido de carga eléctrica positiva.
Modelo nuclear: Los átomos tienen dos partes: el núcleo central, pequeño y compacto, y la corteza alrededor del núcleo y prácticamente vacía. Aspectos a tener en cuenta en este modelo son los siguientes:
- El núcleo está formado por los protones, con carga eléctrica positiva, y los neutrones, eléctricamente neutros.
- El número atómico. Es el número de protones que tiene el núcleo. Se representa con la letra Z y coincide con el número de electrones cuando el átomo es neutro. Todos los átomos de un elemento químico tienen el mismo número atómico.
- El número másico. Es el número total de partículas que hay en el núcleo de un átomo (protones y neutrones). Se representa con la letra A.
- Los isótopos son átomos del mismo elemento que tienen el mismo número atómico, pero distinto número másico.
Los electrones se distribuyen en la corteza en capas o niveles de energía que contienen subniveles. En cada capa pueden situarse: 2 electrones en la 1ª capa (El subnivel s), 8 electrones en la 2ª capa (Dos en el subnivel s y Seis en el subnivel p), 18 electrones en la 3ª capa (Dos en el subnivel s, Seis en el subnivel p y Diez en el subnivel d), 32 electrones en la 4ª capa, etc..
ACTIVIDAD VI: Configuración electrónica de los elementos
Los iones son átomos que ha perdido o ganado electrones en su corteza electrónica. Pueden ser aniones (iones negativos) o cationes (iones positivos).
ACTIVIDAD VII: Átomos y Modelos Atómicos
ACTIVIDAD VIII: Concepto Moderno de Átomo
TABLA PERIÓDICA
Los elementos químicos aparecen clasificados en orden creciente de número atómico en la Tabla Periódica distribuidos a lo largo de 18 columnas o grupos y 7 filas o períodos.
Los átomos, por lo general, se presentan agrupados formando elementos (átomos del mismo número atómico) o compuestos (átomos de distinto número atómico). Las moléculas están formadas por dos o más átomos de un mismo o de diferentes elementos.
Los átomos de los elementos tienden a ganar, perder o compartir electrones para conseguir que su nivel más externo adquiera una configuración más estable. El enlace químico es la unión que se establece entre las partículas elementales que constituyen una sustancia. Existe este tipo de enlaces:
- El enlace iónico es la unión que resulta de la presencia de fuerzas de atracción electrostática entre iones de distinto signo.
- El enlace covalente es la unión de dos átomos que comparten uno o más pares de electrones.
- El enlace metálico es la unión que existe entre los átomos de los metales, que se encuentran formando una red cristalina.
TABLA PERIÓDICA
Presentación "La tabla periódica de los elementos"
ACTIVIDAD: Tabla Periódica y Tipos de Enlaces
CONFIGURACIÓN ELECTRÓNICA
La configuración electrónica indica la forma en la cual los electrones se estructuran u organizan en un átomo, de acuerdo con el modelo de capas electrónicas, que expresa a las funciones de onda del sistema como un producto de orbitales s, p, d y f.
El diagrama de Moeller, también llamado regla de las diagonales,, es una guía utilizada en química para calcular la configuración electrónica de un átomo neutro mediante su número atómico (Z).
Práctica de la configuración electrónica de los elementos
El principio de exclusión de Pauli es una regla que establece, que no puede haber en un átomo dos electrones con todos sus números cuánticos idénticos. En un mismo orbital solamente pueden existir dos electrones y con sus espines opuestos.
El principio de máxima multiplicidad de Hund indica que al llenar orbitales de igual energía (los tres orbitales p, los cinco d, o los siete f) los electrones se distribuyen, siempre que sea posible, con sus espines paralelos, es decir, que no se cruzan. La partícula es más estable cuando tiene electrones desapareados (espines paralelos) que cuando esos electrones están apareados (espines opuestos o antiparalelos).
ACTIVIDAD I: Principios de exclusión de Pauli y de máxima multiplicidad de Hund
ACTIVIDAD II: Orden energético creciente de llenado de electrones
ACTIVIDAD III: Estructuras electrónicas de los átomos
ACTIVIDAD IV: Repasa las configuraciones electrónicas
ACTIVIDAD V: Práctica las configuraciones electrónicas
Los elementos químicos aparecen clasificados en orden creciente de número atómico en la Tabla Periódica distribuidos a lo largo de 18 columnas o grupos y 7 filas o períodos. En cada grupo se colocan elementos con propiedades similares y en cada período se van colocando los elementos en orden creciente de número atómico.
ACTIVIDAD VI: Conoce la Tabla Periódica
ACTIVIDAD VII: Elige tu Tabla Periódica favorita
ACTIVIDAD VIII: Juega al tetris con la Tabla Periódica
ACTIVIDAD IX: Tabla periódica interactiva muy útil
ACTIVIDAD X: 2019 Año Internacional de la Tabla Periódica y de los Elementos Químicos
Recuerda:
"Solamente hay dos tipos de personas, los que se saben la tabla periódica y los que no...."
- El enlace iónico es la unión que resulta de la presencia de fuerzas de atracción electrostática entre iones de distinto signo.
- El enlace covalente es la unión de dos átomos que comparten uno o más pares de electrones.
- El enlace metálico es la unión que existe entre los átomos de los metales, que se encuentran formando una red cristalina.
ACTIVIDAD IX: Tabla Periódica y Tipos de Enlaces
ACTIVIDAD V: Repasa las propiedades periódicas y realiza los ejercicios
ACTIVIDAD VI: Propiedades periódicas I
ACTIVIDAD VII: Propiedades periódicas II
ACTIVIDAD VIII: Ejercicios para practicar las propiedades periódicas
ACTIVIDAD IX: Identifica propiedades
PROPIEDADES PERIÓDICAS
La energía de ionización es la energía mínima que se requiere para arrancar un electrón de un átomo gaseoso en su estado fundamental, transformándolo en un catión.
ACTIVIDAD I: Vídeo Energía de Ionización
La afinidad electrónica es la energía liberada cuando un átomo gaseoso en su estado fundamental incorpora un electrón, transformándose en un anión.
ACTIVIDAD II: Vídeo Afinidad Electrónica
La electronegatividad es la tendencia que tiene un elemento para atraer hacia sí el par electrónico del enlace compartido con otro.
ACTIVIDAD III: Vídeo Electronegatividad
El radio atómico indica la distancia que existe entre el núcleo y el orbital más externo de un átomo. Por medio del radio atómico, es posible determinar el tamaño del átomo.
El radio iónico establece la distancia entre el centro del núcleo del átomo y el electrón estable más alejado del mismo, pero haciendo referencia no al átomo, sino al ion.
ACTIVIDAD IV: Vídeo Radio Atómico y Radio Iónico
Para repasar las propiedades periódicas puedes visitar las siguientes actividades y reflexionar los motivos por los que varían las propiedades periódicas:
ACTIVIDAD V: Repasa las propiedades periódicas y realiza los ejercicios
ACTIVIDAD VI: Propiedades periódicas I
ACTIVIDAD VII: Propiedades periódicas II
ACTIVIDAD VIII: Ejercicios para practicar las propiedades periódicas
ACTIVIDAD IX: Identifica propiedades
ENLACE QUÍMICO
Un enlace químico es la interacción física responsable de las interacciones entre átomos, moléculas e iones, que tiene una estabilidad en los compuestos diatómicos y poliatómico.
En general, el enlace químico fuerte está asociado a la transferencia de electrones de valencia entre los átomos participantes. Las moléculas, cristales, y gases diatómicos está unido por enlaces químicos, que determinan las propiedades físicas y químicas de la materia.
Las cargas opuestas se atraen, porque, al estar unidas, adquieren una situación más estable que cuando estaban separados. Esta situación de mayor estabilidad suele darse cuando el número de electrones que poseen los átomos en su último nivel es igual a ocho, estructura que coincide con la de los gases nobles ya que los electrones que orbitan el núcleo están cargados negativamente, y que los protones en el núcleo lo están positivamente, la configuración más estable del núcleo y los electrones es una en la que los electrones pasan la mayor parte del tiempo entre los núcleos, que en otro lugar del espacio. Estos electrones hacen que los núcleos se atraigan mutuamente.
El enlace químico es la fuerza de unión entre átomos para lograr estabilidad, generalmente completando su última capa de electrones (regla del octeto). Existen tres tipos principales basados en la transferencia o compartición de electrones: iónico (metal + no metal, transfiere electrones), covalente (no metal + no metal, comparte electrones) y metálico (metal + metal, "mar" de electrones).
Los átomos buscan ser más estables, alcanzando una configuración electrónica similar a la de un gas noble (generalmente 8 electrones en la última capa), lo que reduce su energía total, formando tres tipos de enlaces:
Enlace Iónico (Metal + No metal):
- Ocurre por transferencia de electrones del metal al no metal.
- Forma cationes (+) y aniones (-).
- Se unen por fuerzas electrostáticas, formando redes cristalinas (sólidos), no moléculas.
- Propiedades: Altos puntos de fusión, solubles en agua, conducen la electricidad disueltos o fundidos.
Enlace Covalente (No metal + No metal):
- Los átomos comparten electrones para completar su capa.
- Forman moléculas (unidades pequeñas) o redes covalentes.
- Propiedades: Bajos puntos de fusión (suelen ser gases o líquidos), no conducen la electricidad, insolubles en agua (generalmente).
Enlace Metálico (Metal + Metal):
- Los átomos metálicos liberan electrones, creando un "mar" de electrones deslocalizados que rodean a los cationes.
- Propiedades: Buenos conductores de electricidad y calor, maleables, dúctiles y con alto punto de fusión.
Para repasar el tema de enlace químico de 4ºESO puedes descargar la presentación:
Presentación Enlace Químico
ENLACE COVALENTE: MOLÉCULAS COVALENTES Y SÓLIDOS COVALENTES
ACTIVIDAD I: Simulador Enlace Covalente
ACTIVIDAD II: Simulador de moléculas polares y apolares
ACTIVIDAD III: Juega con los enlaces
ACTIVIDAD III: Juega con los enlaces
Denominamos estructura de Lewis al esquema en el que aparecen todos los átomos de la molécula con sus electrones de la última capa y en la que vemos tanto los pares compartidos o enlaces covalentes, como los no compartidos o pares no enlazantes.
Los pasos a seguir son:- Realizar la configuración electrónica de los átomos para conocer cuántos electrones de valencia tienen.
- Saber los enlaces que quiere formar cada uno de los átomos, serán los mismos que electrones le falten para completar el octeto.
- Dibujar esos pares enlazantes y añadir los pares no enlazantes a cada átomo para que aparezcan todos sus electrones de la última capa.
ACTIVIDAD IV: Vídeo estructura de Lewis Teoría y Ejercicios
ACTIVIDAD V: Construye diagramas de Lewis
Las estructuras resonantes son útiles porque permiten representar moléculas, iones y radicales para los cuales resulta inadecuada una sola estructura de Lewis. Se escriben entonces dos o más de dichas estructuras y se les llama estructuras en resonancia o contribuyentes de resonancia.
ACTIVIDAD VI: La resonancia en química
ACTIVIDAD VII: Resonancia del benceno
ACTIVIDAD VIII: Estructuras resonantes
Para que una molécula sea polar, debe tener átomos con diferente electronegatividad y separación de cargas en la moléculas, con estas dos premisas en la molécula habrá un momento dipolar en la molécula.
Los compuestos covalentes diferenciaremos entre las propiedades de las moléculas y los cristales.
Los compuestos covalentes moleculares:
Los cristales covalentes :
Los compuestos covalentes moleculares:
- Tienen puntos de fusión y ebullición bajos debido a que las fuerzas entre las moléculas son débiles, siendo mayores cuando aumenta la polaridad.
- No conducen la electricidad ya que no hay cargas ni electrones libres.
- Se disuelven en sustancias con su misma polaridad, es decir, si es apolar en disolventes apolares y en polares cuando sea polar.
ACTIVIDAD XI: Propiedades de compuestos covalentes moleculares
- Tienen altos puntos de fusión y ebullición por estar los átomos unidos por enlaces covalentes bastante fuertes.
- Son insolubles en casi todos los disolventes.
- No conducen el calor ni la electricidad, a excepción del grafito que dispone de electrones que pueden moverse entre las capas planas.
Este vídeo y las actividades siguientes te pueden servir para repasar la formación y las propiedades del enlace covalente:
ACTIVIDAD XIII: Repasa el enlace covalente I
ACTIVIDAD XIV: Repasa el enlace covalente II
ENLACE IÓNICO: CRISTALES IÓNICOS
El enlace iónico es el resultado de la fuerzas de atracción electrostática entre iones de distinto signo.
Un enlace se considera iónico cuando la electronegatividad de los elementos que forman el enlace es superior a 1,8.
ACTIVIDAD I: Simulador de Enlaces
ACTIVIDAD II: Juego del enlace iónico
Los compuestos iónicos forman redes cristalinas constituidas por un número enorme de iones de carga opuesta, unidos por fuerzas electrostáticas. Este tipo de atracción determina las propiedades observadas. Si la atracción electrostática es fuerte, se forman sólidos cristalinos de elevado punto de fusión e insolubles en agua; si la atracción es menor, como en el caso del NaCl, el punto de fusión también es menor y, en general, son solubles en agua e insolubles en líquidos apolares, como el benceno.
ACTIVIDAD III: Redes iónicas cristalinas
ACTIVIDAD IV: Redes iónicas
ACTIVIDAD V: Resumen de las propiedades del enlace iónico
La energía de red o energía reticular es la energía que se desprende al fomarse un mol de cristal iónico a partir de los iones que lo componen en estado gaseoso. Para calcular la energía reticular se puede usar la ecuación de Born-Landé
ACTIVIDAD VI: Parámetros de los que depende la energía de red
Mediante el ciclo de Born-Haber es posible calcular el valor de la energía reticular utilizando un camino indirecto basado en la ley de Hess, sin más que sumar los cambios de energía que tienen lugar en el proceso de formación del compuesto iónico.
ACTIVIDAD VII: Vídeo del ciclo de Born-HaberACTIVIDAD VIII: Ciclo de Born-Haber
ACTIVIDAD IX: Ejemplos del Ciclo de Born-Haber
Este vídeo y las actividades siguientes te pueden servir para repasar la formación y las propiedades del enlace iónico:
ACTIVIDAD X: Repasa el enlace iónico
ENLACE METÁLICO: REDES METÁLICAS
Un enlace metálico es un enlace químico que mantiene unidos los átomos de los metales entre sí. Existe la unión entre núcleos atómicos y los electrones de valencia, que se juntan alrededor de éstos núcleo atómicos y forman la nube electrónica En el enlace metálico todos los átomos comparten los electrones del nivel más externo, dando lagar a redes cristalinas metálicas.
Los compuestos metálicos se ordenan redes tridimensionales, ocupando posiciones de equilibrio en los vértices de determinadas formas geométricas. Los metales de uso industrial más frecuente cristalizan en tres redes que son:
ACTIVIDAD V: Construye redes metálicas
- Red cúbica centrada en el cuerpo, con una coordinación de 8 como el litio o sodio.
- Red cúbica de caras centradas, con una coordinación de 12 como el oro, aluminio o plomo.
- Red hexagonal compacta, con una coordinación de 12 como magnesio, cinc o cadmio.
ACTIVIDAD V: Construye redes metálicas
Para explicar el enlace metálico se utilizan dos modelos:
- Modelo del mar de electrones, en el que se afirma que los electrones de valencia no pertenecen a los átomos del metal, sino que todos ellos forman lo que se conoce como "mar de electrones", estando deslocalizados por toda la red y siendo comunes al conjunto de átomos que la forman.
- Modelo de bandas, según el cual se describe la estructura electrónica del metal como una estructura de bandas electrónicas, o simplemente estructura de bandas de energía, debidas al solapamiento de los orbitales atómicos. Existiendo dos bandas una de valencia ocupada por los electrones de valencia de los átomos, es decir, aquellos electrones que se encuentran en la última capa o nivel energético de los átomos y otra banda de conducción que está ocupada por los electrones libres, es decir, aquellos que se han desligado de sus átomos y pueden moverse fácilmente. Estos electrones son los responsables de conducir la corriente eléctrica y en función de la distancia entre las capas de valencia y conducción se pueden clasificar los materiales como conductores, semiconductores o aislantes.
ACTIVIDAD VI: Vídeo del modelo de mar de electrones
ACTIVIDAD VII: Modelo de la teoría de bandas
Los metales son todos, salvo el mercurio, sólidos a temperatura ambiente, tienen alta conductividad térmica y eléctrica, poseen brillo metálico, son dúctiles y maleables y emiten electrones por efecto del calor y la luz.
ACTIVIDAD VIII: Resumen de las propiedades del enlace metálico
Este vídeo y las actividades siguientes te pueden servir para repasar el enlace metálico:
LAS FUERZAS INTERMOLECULARES
Las fuerzas que tienden a unir las moléculas de compuestos covalentes se denominan fuerzas intermoleculares.
ACTIVIDAD I: Simulación de las fuerzas intermoleculares
Como las moléculas covalentes pueden ser polares y apolares a estas fuerzas se las clasifica de la siguiente manera:
- Fuerzas dipolo-dipolo (moléculas polares)
- Fuerzas de London (moléculas apolares o dipolos instantáneos)
- Enlace de hidrógeno (moléculas con atómos de hidrógeno unidos a átomos de flúor, oxígeno o nitrógeno)
ACTIVIDAD III: Vídeo de enlace de hidrógeno
ACTIVIDAD IV: Resumen de las fuerzas intermoleculares I
ACTIVIDAD V: Resumen de las fuerzas intermoleculares II
Este vídeo te explica con detalle las fuerzas intermoleculares
FORMULACIÓN Y NOMENCLATURA
Para
representar una sustancia química utilizaremos la fórmula química que
nos indicará los tipos de átomos que la forman así como el número o
proporción de estos átomos en dicha sustancia.
El
objetivo de la formulación y nomenclatura química es que a partir del
nombre de un compuesto sepamos cuál es su fórmula y a partir de una
fórmula sepamos cuál es su nombre. Antiguamente esto no era tan fácil,
pero gracias a las normas de la I.U.P.A.C. la formulación puede llegar a
ser incluso entretenida.
Cuando
estudiamos las configuraciones electrónicas de los átomos vimos que los
electrones de la capa de valencia tenían una importancia especial ya
que eran los que participaban en la formación de los enlaces y en
las reacciones químicas. También vimos que los gases nobles tenían gran
estabilidad, y eso lo achacábamos a que tenían las capas electrónicas
completas. Pues bien, tener las capas electrónicas completas será la
situación a que tiendan la mayoría de los átomos a la hora de formar
enlaces, o lo que es lo mismo a la hora de formar compuestos.
Os dejo estos enlaces para practicar Nomenclatura y Formulación
Formulación FisQuiWeb
Formulación AlonsoFormula
Ejercicios de Formulación
Ponencia sobre Formulación y Nomenclatura Universidad de Sevilla
Orientaciones PAU 2012 Madrid
Apps para móviles
LAS REACCIONES QUÍMICAS
ACTIVIDAD: Simulación de la Precipitación del Diyoduro de plomo
Según la teoría de colisiones para que tenga lugar una reacción química es necesario:
- Energía suficiente para que se rompan los enlaces entre átomos de reactivos. La energía mínima necesaria para que se produzca la reacción se denomina energía de activación.
- Orientación adecuada para que, al romperse los enlaces, los átomos libres se puedan unir de la manera que requiere la formación de productos.
Una ecuación química es la representación escrita y abreviada de una reacción química. Ajustar una reacción química consiste en asignar a cada fórmula un coeficiente para que haya el mismo número de átomos de cada elemento en ambos miembros.
ACTIVIDAD: Ajuste de reacciones I
ACTIVIDAD: Ajuste de reacciones II
ACTIVIDAD: Ajuste de reacciones III
ACTIVIDAD: Ajuste de reacciones I
ACTIVIDAD: Ajuste de reacciones II
ACTIVIDAD: Ajuste de reacciones III
Según la ley de conservación de la masa en una reacción química, la suma de las masas de todas las sustancias que intervienen se mantiene constante. Es decir, la suma de las masas de los reactivos es igual a la suma de las masas de los productos.
Cuando trabajamos con gases según la hipótesis de Avogadro, volúmenes iguales de cualquier gas, medidos en las mismas condiciones de presión y temperatura, contienen el mismo número de moléculas.
La velocidad de reacción es la rapidez con la que se combinan los reactivos o la rapidez con la que se forman los productos, la velocidad de reacción depende de diversos factores como son la temperatura, la concentración de los reactivos, el grado de división de los reactivos sólidos y la presencia de catalizadores.
En una reacción química, siempre tiene lugar un intercambio de energía entre las sustancias que intervienen y el medio en el que se encuentran. Según sea el sentido del intercambio de energía estas pueden ser:
- Reacciones endotérmicas tienen lugar con absorción de energía en forma de calor.
- Reacciones exotérmicas transcurren con desprendimiento de energía en forma de calor.
Si conocemos la masa y el volumen de algunos de los reactivos o productos de reacción, podremos calcular la masa y el volumen de las demás sustancias de la reacción. Para obtener esta información cuantitativa, efectuamos cálculos estequimétricos, que resolveremos aplicando factores de conversión.
Procedimiento para efectuar cálculos estequimétricos:
Procedimiento para efectuar cálculos estequimétricos:
- Escribimos y ajustamos la ecuación química correspondiente.
- Convertimos a moles el dato de partida.
- Aplicamos la relación molar entre la sustancia conocida y la que queremos conocer, según los coeficientes de la ecuación química ajustada.
- Calculamos la masa o el volumen de la sustancia requerida.
ACTIVIDAD: Repaso del tema QuimicaWeb
ACTIVIDAD: Repaso del tema ANAYA
QUÍMICA ORGÁNICA
La química orgánica es la química del carbono y de sus compuestos. Estos compuestos de carbono se encuentran formando enlaces covalentes carbono-carbono o carbono-hidrógeno y otros heteroátomos, todos estos compuestos son los que llamamos compuestos orgánicos. Debido a la omnipresencia del carbono en los compuestos que esta rama de la química estudia esta disciplina también es llamada química del carbono.
La química orgánica tiene una gran importancia debido a que los seres vivos estamos formados por moléculas orgánicas, proteínas, ácidos nucleicos, azúcares y grasas. Todos ellos son compuestos cuya base principal es el carbono. Los productos orgánicos están presentes en todos los aspectos de nuestra vida: la ropa que vestimos, los jabones, champús, desodorantes, medicinas, perfumes, utensilios de cocina, la comida, etc.
EJERCICIOS INTERACTIVOS (Alonso-Formula)
"Existen dos tipos de personas en la vida los que saben la tabla periódica y los que no"
"Existen dos tipos de personas en la vida los que saben la tabla periódica y los que no"
Ejercicios repaso 4ºESO Física y Química
Ejercicios Santillana 4ºESO
Ejercicios Anaya 4ºESO
- La actividad científica
- El átomo y el sistema periódico
- Enlace químico y fuerzas intermoleculares
- Los compuestos del carbono
- Reacciones químicas fundamentos
- Reacciones químicas de interés
- Cinemática
- Leyes de Newton
- Fuerzas en el Universo
- Fuerzas en fluidos. Presión
- Energía mecánica y trabajo
- Energía térmica y calor
Estándares evaluables de aprendizaje:
.png)


.gif)









.png)









No hay comentarios:
Publicar un comentario